跟腱病理学与跟腱断裂(Achilles Pathology and Ruptures)
一、解剖
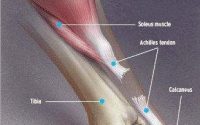
跟腱是全身最大也是最粗壮的腱性结构,由小腿三头肌肌腱(由腓肠肌内、外侧头和比目鱼肌构成)和跖肌组成。但有一部分人的跟腱仅由小腿三头肌肌腱构成,占总人口的6%~8%。跟腱很特别,在其向远端走行过程中旋转90°,远端止于跟骨后上结节。
与其他部位的肌腱不同,跟腱并没有真正意义上的滑膜鞘。跟腱被膜由腱旁组织(分为脏层和壁层)、跟腱系膜、外膜、内膜组成。穿动脉走行于被膜前方,并穿透前方被膜滋养跟腱。被膜内表面具有多个由薄层黏多糖构成的润滑结构,便于跟腱在被膜中滑动,最大的相对滑动距离约为1.5cm。腱鞘由富含血管的结缔组织构成。
对跟腱血液供应的良好理解对手术医师而言非常重要。胫后动脉返支经腱腹交界处滋养跟腱近端部分;胫前动脉跟骨支在腓骨后方发出数根穿动脉滋养跟腱远端部分;在跟腱止点以近2~6cm为以上两供血区的分界线。核医学研究表明,跟腱在这一范围的血液供应是最差的:跟腱止点以近4cm开始,跟腱内血管明显减少。进一步的研究还表明,随着年龄的增长,跟腱的供血血管数量会进一步减少。这也许是造成跟腱损伤风险随着年龄增加而升高的原因。
许多跟腱疾病与其周围结构病变密切相关。跟腱周围有两个重要的囊性结构,跟骨后囊位于跟腱前方、跟骨结节后上方足背伸时该囊压强增大,而跖屈时压强减小。跟腱表面滑囊位于跟腱后方、皮肤及皮下组织深层。这一滑囊的形成与该部位容易受到持续外部刺激(如穿鞋时的慢性刺激)有关。对Haglund畸形(跟骨外侧壁后上方的异常突起)的患者而言,他们更容易发生跟骨后滑囊炎和跟腱机械性刺激损伤。
跟腱主要由胶原蛋白、弹性蛋白、黏多糖、糖蛋白构成。跟腱内的成熟的成纤维细胞产生Ⅰ型和Ⅲ型胶原。正常跟腱的95%由Ⅰ型胶原构成。跟腱断裂后,跟腱中Ⅲ型胶原的比例升高,最终可能导致跟腱愈合后强度下降。随着年龄的增长,跟腱中成纤维细胞密度、胶原纤维直径和胶原纤维密度下降,引起跟腱纤维强度下降。年纪越大的运动员跟腱损伤的风险越高,原因正在于此。
二、生物力学
小腿三头肌依次跨过膝关节、踝关节和距下关节;在步态的蹬离期时,能够帮助屈膝和跖屈踝;它还能够帮助足旋后。研究表明跟腱能够承受的载荷是全身最大的。全速奔跑时,跟腱承受载荷的峰值是体重的12.5倍(约9000N);跳跃或转圈时,跟腱承受载荷的峰值则能达到1000~4000N。跟腱对于机械性刺激非常敏感,因此,经常运动能够促使跟腱直径增加,而活动较少则造成跟腱直径减小。同时,年龄的增加与缺乏锻炼能够导致跟腱强度下降,而经常运动则能促进跟腱强度增加。多项研究表明,过度的刺激会导致退行性酶分泌增加,而缺乏刺激则会导致细胞外基质退变和降解,都会引起跟腱质量的下降。通过控制运动量,能够有效地增加胶原蛋白含量、增加胶原纤维的直径,进而提高跟腱的质量。
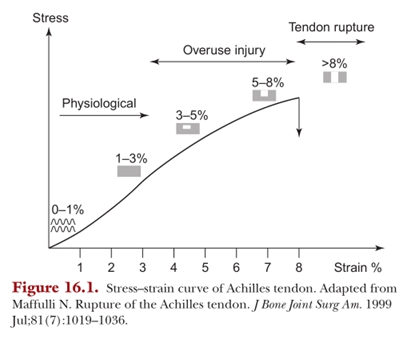
图16.1是跟腱应力应变曲线的详细记录。在静息状态下,曲线显示跟腱的拉伸强度逐渐减低。研究表明,胶原纤维形变程度与跟腱载荷呈线性相关作用于跟腱的张力小于4%时(绝大多数的生理负荷在此范围内),胶原纤维没有明显的变化;4%~8%的张力会导致分子间交叉连接失效,胶原纤维间发生相对滑动;张力超过8%时,胶原纤维承受的张力和纤维间的剪切应力过大,最终造成宏观层面的跟腱断裂。
三、诊断
在怀疑跟腱损伤时,我们需要详细地询问病史,包括受伤机制、既往受伤史、并发症(如糖尿病和肾病)、用药史(如氟喹诺酮类药物和糖皮质激素注射史)、社会史(如吸烟和类固醇摄入),这都将有助于明确诊断和制定治疗方案。体格检查应当包括完善的下肢检查和针对跟腱损伤的特征性检查。特征性的体征包括瘀斑、水肿、跟腱走行区域的张力减低或张力缺失。同时我们也应当完善外周血管病变和外周神经病变的检查和评估。检查的范围应当还包括膝、踝和距下关节。
当我们疑诊跟腱断裂时,应当考虑到长屈肌腱和趾长屈肌腱在踝跖屈时的作用,避免被体检中假阴性的结果蒙蔽。患者应当保持俯卧位,膝关节屈曲90°;这时检查者挤压患者小腿后方肌肉,同时观察踝关节跖屈的情况。如果此时没有观察到踝关节的跖屈,则此项检查为阳性。体检的时候我们还应当注意比较健侧静息位的跟腱张力,以及挤压腓肠肌时踝关节跖屈的程度:而且,我们还应当考虑到,对于在腱腹交界处或以近发生腓肠肌撕裂的患者,Thompson试验可能为假阳性。
在观察影像学资料时,应当尽可能地考虑到所有的跟腱损伤的影像学变化。阅片时应当首先除外骨折可能,同时注意观察是否存在Kager三角区缺损——在侧位片上可以看到长屈肌腱与跟腱之间的透亮三角形。超声检查已经被证明是明确跟腱炎诊断和评估治疗效果的有效手段,也同样适用于跟腱断裂的诊断。MRI对跟腱变性,腱周炎,急、慢性跟腱断裂的诊断都有帮助。特別是有助于对慢性跟腱撕裂断端间隙的评估。
四、跟腱疾病
跟腱疾病通常伴有不同程度的各种不适:疼痛、肿胀、跟腱功能下降。这与跟腱中胶原蛋白的结构变化密切相关——胶原纤维平行排列序列紊乱、纤维间相互分离、纤维直径与密度减少,同时3型胶原蛋白的含量明显增加。由于强度和刚度减低,跟腱会逐渐增生肥厚以图代偿功能;但是持续增加的应变和断裂伸长率导致杨氏模量持续下降,最终形成了更加肥厚、更富有弹性但承受载荷能力更小的跟腱。
跟腱疾病的确切病因现在尚未明确。但是它的发生与跟腱的过度使用和其他许多自然因素相关(比如宿主易感性和生物力学异常)弓形足、后足内翻、伸膝位踝背伸受限或过度旋前、距下关节活动受限、足内翻的患者发生跟腱疾病的风险更高。下肢长度差异超过5mm的运动员、或者下肢长度差异超过20mm的普通人更易于发生跟腱疾病。肌无力或肢体力量、耐力、灵活性的不协调,同样也能增加跟腱疾病的发生风险。
(一)跟腱非止点腱病(NIAT)
NIAT包括跟腱炎、腱周炎、跟腱-腱周炎。虽然理解这三个诊断的不同之处十分重要,但如表16.1所示,它们的检查和治疗通常都是相同的。
1、发病机制
确切的发病机制目前仍不明确。它在运动员中发病率高,通常与过度使用、运动习惯改变(包括运动频度和持续时间的改变)、缺乏运动技巧、运动环境恶劣、受力方式改变、更换运动鞋有关。患有NIAT的田径选手中,有60%~80%采用了错误的训练方式。因此,也有人将病因归结为:“(运动)太多、太早、太快”。
| 表16.1跟腱炎性疾病的鉴别 | |
| 跟腱炎 | 跟腱变性(包括老化、微损伤、血管损伤)引起的跟腱增厚;组织病理学可见细胞脂肪变性、缺氧降解,无炎性细胞浸润 |
| 腱周炎 | 腱旁组织的炎性病变和增厚;组织病理学可见炎性细胞浸润 |
| 跟腱炎合并腱周炎 | 跟腱变性与腱旁组织炎症并存;组织病理学同时可见腱周炎和跟腱炎的表现 |
跟腱变性循环由一系列逐渐导致NIAT恶化的事件构成(图16.2)。反复作用的应力能够导致损伤无法完全修复,并能破坏胶原交联。组织变性将导致炎性反应的发生和易伤性的增加,从而促使这一过程不断循环。我们有理由相信,动脉供血减少、局部缺氧、代谢缺陷、自由基形成和运动引起的高体温都可能诱发跟腱变性,但这一点目前仍存在争议。
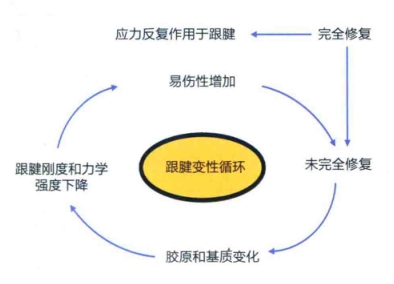
图16.2跟腱变性循环
2、临床表现
跟腱疾病通常表现为运动相关的跟腱区域疼痛,疼痛的区域常见于跟腱止点上方2~6cm的范围。早期的症状包括疼痛、肿胀、发热这类单纯的NIAT表现。无论在休息时或运动中,这些症状将逐渐变得频繁发作。为了缓解症状,控制患者的运动量是必要的。跟腱炎合并腱周炎时,症状将比单纯的跟腱炎或腱周炎更明显。
查体时,在跟腱止点上方2~6cm可扪及跟腱空虚感,局部或可扪及结节并伴有发热和肿胀。跟腱炎的患者可以在跟腱处扪及伴随跟腱滑动的无痛结节;而腱周炎的患者可以在跟腱周围扪及不伴随跟腱滑动的痛性结节。NIAT的患者还会表现出加速跑时力量下降、踝背伸增加、踝跖屈受限。评估患者生物力学变化的情况非常重要,包括下肢长度差异、踝关节不稳定性、骨性序列紊乱、韧带松弛、韧带僵直或挛缩。以上这些都能增加NIAT的发生风险(图16.3)。
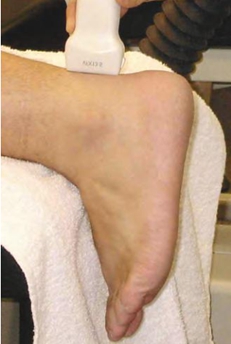
图16.3跟腱的临床检查
3、诊断
影像学检查包括X线、超声检查(图16.4)和MRI。影像学检查多数情况下都是正常的,但有时也能显示出跟腱内的钙化。
超声检查是一种操作简单、检查速度快、成本低廉的检查方式。同时它还能用于跟腱疾病的治疗,如超声引导下的局部注射。超声检查的缺点包括:因使用者不同导致检查结果存在差异、仅限于软组织的检查、与MRI相比敏感性低。超声下正常的跟腱表现为同质纤维结构,与周围腱旁组织间有明显的边界(4~7mm厚)。跟腱炎患者的跟腱在超声下可见纺锤形增厚,病变区域呈低回声信号;在多普勒超声检查中可见跟腱内新生血管形成。研究表明,普通人群中有28%的个体存在跟腱微撕裂;在运动员中,则有82%的个体存在这样的病变。腱周炎患者的跟腱显影正常,但在跟腱周围可见低回声区域,腱旁组织内可见丰富的血流信号。
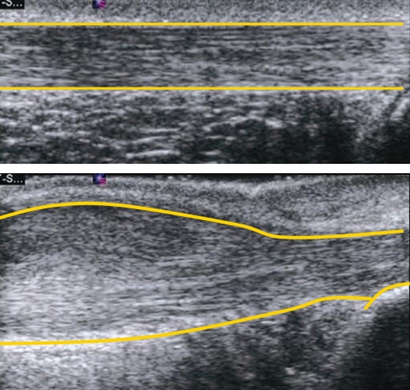
图16.4 超声检查中正常的跟腱影像(上)与呈纺锤形增厚的异常跟腱影像(下)
虽然MRI检查对于NIAT的诊断而言并不是必须的,但由于成像灵敏度高,它通常是影像学研究的首选检查(图16.5)。MRI影像能够提供更好的组织对比和更髙的空间分辨率,从而让我们能更好地识别解剖结构和进行病理学评估分级。MRI检查的缺点包括花费高、普及困难、检查时间长。跟腱炎患者的MRI影像,可以看见纺锤形增厚(前后径较正常直径增加约6mm)的跟腱,同时伴有跟腱内信号改变。在腱周炎患者的影像中,T2相中可见腱旁组织内高信号和正常显影的跟腱。
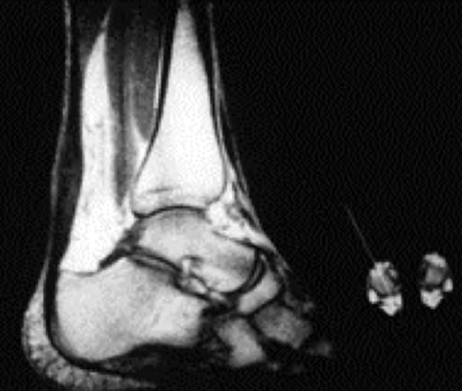
图16.5 MRI显示出纺锤形增厚的跟腱。这是由于跟腱内Ⅲ型胶原蛋白含量增高引起的。
4、非手术治疗
评估NIAT治疗效果的统计数据研究结果不一。但是在表16.2中可以看到,非手术治疗是经典的首选治疗方式。非手术治疗包括休息和活动限制、非甾体抗炎药、具有舒张血管作用的乳霜、冷敷、肢体制动、离心运动、交叉训练、伸展运动、冲击波治疗、减少危险因素(包括垫高鞋跟及使用矫形器)等(图16.2)。虽然没有标准的治疗流程,但通常情况下,患者都被要求制动患肢2~6周,然后再接受其他更多的治疗和康复训练。超过90%的急性N1AT患者经非手术治疗症状能得到缓解,但慢性患者有效率则相对较低。
离心运动指收缩肌肉使跟腱伸展延长。在这一过程中产生的伸展应力能够使跟腱内血流减少,从而减少新生血管和与之相关的痛觉感受器的形成。经过12周的离心运动练习,能够有效地缓解症状。冲击波治疗通过刺激软组织修复、促进跟腱纤维重组、抑制痛觉感受器来缓解疼痛。冲击波将能量注入细胞内造成细胞内损伤,增加细胞膜渗透性,促使神经细胞去极化,从而阻止疼痛信号的传导冲击波疗法可以通过多种途径治疗跟腱损伤,但也是非常昂贵的。
具有舒张血管作用的乳霜含有硝酸甘油,可以释放出具有促进成纤维细胞胶原分泌作用的一氧化氮;但是它同时也会诱发血管性头痛,从而降低患者的依从性。通常不推荐这一治疗方案。其他针对NIAT的非手术治疗方法包括糖皮质激素注射、富血小板血浆(PRP)注射和普罗疗法(增生疗法)。这些治疗方法的侵入性更强,而且没有足够的数据证明它们足够有效。糖皮质激素注射可在短时间内缓解疼痛,但是跟腱内注射能导致跟腱代谢异常。我们尤其反对进行类固醇注射。PRP注射也许能够通过细胞因子作用促进修复,但迄今为止尚无明确的证据证实其有效性。普罗疗法包括注射硬化剂或聚多卡醇,药物作用于血管内膜促使血栓形成,进而破坏局部神经缓解疼痛,但该疗法的疗效因人而异。
5、手术治疗
手术治疗通常仅用于治疗经非手术治疗无法缓解的难治性跟腱疾病。在选择手术治疗之前,应至少尝试3个月的非手术治疗。腱周炎的手术治疗主要是通过对肌腱和腱旁组织的松解术、或切除腱旁组织的清创术来实现。跟腱炎的手术治疗则包括清创术、微创手术、长屈肌腱移位术。即便通过手术治疗,仍有25%~50%的NIAT患者无法得到治愈。
手术的目的是切除退变组织和促进损伤愈合,必要时也可行带血管的肌腱移植。当跟腱病变超过30%~50%时,建议通过行长屈肌腱移植术来强化跟腱。首选长屈肌腱移植的原因除了它血运良好外,还在于它在踝跖屈过程中所起的作用与跟腱相似。Topaz清创术可以借助微型电刀经由一个1.5cm的皮肤切口完成。从理论上讲,在退变组织的不同层面灼烧穿孔可以促进局部新生血管的形成。
接受手术治疗的患者中,约10%会发生并发症。但术后1年时,绝大多数患者都对治疗效果感到满意,并能恢复患病前的活动强度。并发症包括皮肤坏死、浅层或深部感染、积液和血肿形成、腓肠神经损伤、新发跟腱断裂、深静脉血栓形成(DVT)、过度敏感的或增生肥厚的瘢痕。Maffulli认为,女性患者预后相对欠佳,她们术后并发症更多,,恢复时间更长,二次手术率更高。
(二)、跟腱止点腱病
与NIAT相类似,跟腱止点腱病包括一系列累及跟腱止点(包括跟骨后上部及邻近区域)的腱病,如:跟骨后滑囊炎、跟腱后滑囊炎、Haglund畸形、跟腱止点腱周炎、跟腱止点跟腱炎、全身性肌腱端病。
1、病因学
充分考虑上述多种疾病同时发生的可能是非常重要的,事实上它们也的确经常同时发生。比如Haglund畸形(指跟骨外侧壁后上结节的异常增大)会撞击跟腱止点纤维束和跟腱囊引发多种疾病。Haglund畸形并非是引发这类病理变化的唯一原因,滑囊炎、跟腱撞击也可能引发腱周炎和跟腱止点炎(关于这一点仍存在争议)。Kang等已经证明Haglund畸形并不是诱发跟腱止点炎的必要条件。跟腱止点内的钙化可以提示这一区域内发生的退行性改变。
作用于跟腱的恒定的、持续的负荷能够引发跟腱炎(如跟腱变性、滑囊炎、Haglund畸形等),这是一个真正的炎性浸润过程。高发人群为肥胖患者以及老年业余运动员。位于跟腱与跟骨后突间的跟骨后滑囊在长期的冲击下会发生跟骨后滑囊炎。位于跟腱与皮肤间的跟腱周围滑囊在反复冲击下则会发生跟腱后滑囊炎。这通常是由鞋子上的突起反复摩擦撞击跟腱局部引起的。
跟腱止点炎的患者相当部分是较年长的业余运动爱好者。这部分患者的发病机制则是跟腱附着端病变。相对于年轻男性患者而言,他们可能更多地受到银屑病、痛风、脊柱关节病等基础疾病的影响。该病通常双侧发病。这些内容已经超出了本章所探讨的内容,但遇到该病患者时应当考虑到上述的情况。
2、临床表现
典型病例为较年长的运动爱好者,他们通常被称为“周末勇士”(指仅在周末进行体育活动的人群)。症状通常包括肿胀、逐渐加重的钝痛或提踵时跟腱局部的疼痛。症状在运动后或穿鞋时加重。在山间跑步、运动强度变化或运动失误时也可感到症状加剧。踝背伸时压迫位于跟腱和跟骨间的跟后滑囊会感觉疼痛明显加重。体格检查时应注意跟腱止点局部的触诊,并评估肿胀情况及皮温。对于跟腱挛缩的患者,Silfverskiold试验能够显示跟腱止点紧张的程度。
3、诊断
与NIAT相似,跟腱止点炎的诊断包括X线、B超、MRI。X线有助于评估跟骨的解剖形态,判断是否存在Haglund畸形、肌腱钙化以及测量后跟骨角度和PPLs(用于确定是否存在Haglund畸形)。
超声能够明确显示跟腱内钙化、跟腱异常增厚以及跟腱止点炎(图16.6)。对于跟骨后滑囊炎以及跟腱周围滑囊炎的患者,超声能够清晰地显示出囊内的滑液和增厚的囊壁。
MRI在显示跟腱、滑囊、骨性畸形和疾病进展程度方面非常有价值。影像特点与NIAT非常相似,但位于跟腱止点局部。另外,MRI还能清晰地显示出逐渐增加的囊液和滑囊周围的炎性改变。在对跟腱断裂的成像上也更为敏感。
| 表16.2 治 疗 | ||
| 治 疗 | 预 期 | |
| 最初的报告 | 足跟抬高(牛仔靴、高跟鞋),NSAIDs,训练修正 | 适当运动可综合改善 |
| 3-6个月 | 物理疗法,应注重离心训练 | 可触及的大结节消失 |
| 手 术 | 切开清创或等离子刀清创 | 恢复性锻炼至少9个月 |
4、治疗
跟腱止点炎的早期治疗与其他部位的跟腱炎类似。非手术治疗对于将近90%的病例都能取得满意的疗效。通过表16.3可以发现,通过服用非甾体抗炎药(NSAIDs)、物理治疗、解除鞋的压迫、改变训练方法或降低强度等非手术治疗方法,其余的患者也能部分改善症状。治疗时应避免注射皮质类固醇以降低跟腱断裂的风险。
| 表16.3 跟腱止点眼的治疗 | ||
| 治 疗 | 预 期 | |
| 最初的报告 | 足跟抬高(牛仔靴、高跟鞋),NSAIDs,训练修正 | 适当运动可综合改善 |
| 3-6个月 | 物理疗法(离心训练训练效果不显著) | 综合改善,特别是在X线影像中课件钙化的患者 |
| 手 术 | 切开清创,Haglund切除及复位 | 恢复性锻炼至少9个月 |
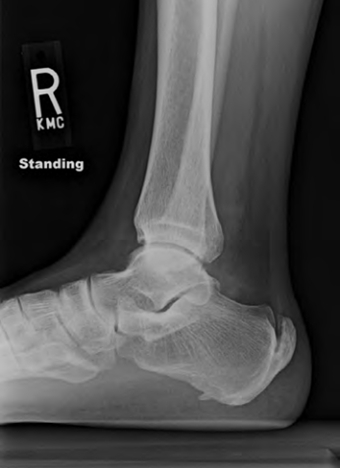
图16.6跟腱内钙化往往预示跟腱炎非手术治疗疗效欠佳
手术治疗适用于难治性跟腱止点炎的患者。手术通常仅限于病变局部,包括Haglund畸形的切开截骨或镜下截骨(图16.7)、滑囊切除、局部清创;如果跟腱止点病变超过50%,则须行长屈肌腱移位。如在X线图像上可见明显的跟腱内钙化,则应使用缝合锚重建跟腱止点,建议使用双排构建以增加强度。
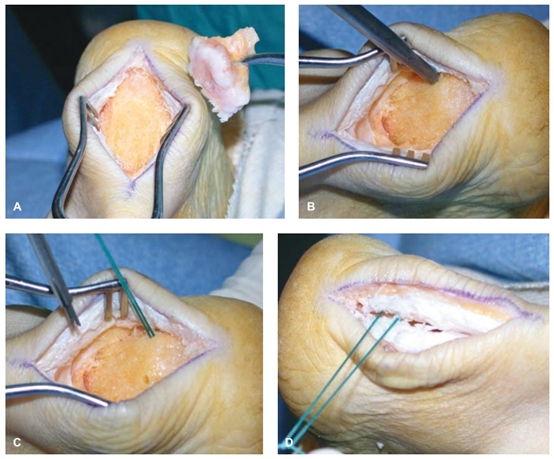
图16.7 Haglund畸形截骨术。 A.切除骨突; B-D.用带线锚钉重建止点(单排构建或双排构建)
(三)急性跟腱断裂
跟腱断裂的发病率在工业化国家持续增长,究其原因在于人们越来越少的日常运动和出现越来越多的“周末勇士”(仅在周末参加体育活动的人群)。高发年龄为30~40岁;随着年龄的增长,男女比例从2:1逐渐变为19:1。75%的急性跟腱断裂与运动相关。左侧发病率高于右侧:这可能是由于右腿习惯于将重量推向左腿导致的。值得注意的是,80%的跟腱断裂都发生于跟腱止点以上2~6cm的范围内。跟腱断裂的高危因素包括久坐的生活习惯、皮质类固醇注射(导致局部胶原蛋由坏死)、合成代谢类固醇的使用(导致胶原异常增生进而使跟腱强度降低)、甲状腺功能亢进症、肾功能不全、痛风、动脉粥样硬化、氟喹诺酮类药物的使用。此外,系统性疾病引起的跟腱轻微损伤同样可以增加断裂风险。
急性跟腱断裂通常发生在机械超负荷作用于逐渐变性的跟腱时。久坐会导致跟腱局部血管减少,进而使微损伤难以修复愈合;这样的损伤逐渐积累最终导致宏观的断裂。支持这一理论的依据是:15%的患者在跟腱断裂前就存在局部症状。
1、临床表现
急性跟腱断裂的典型表现包括后踝疼痛、提踵困难、跖屈无力以及受伤时听见断裂声。受伤的机制可能是在比目鱼肌收缩的情况下踝关节迅速背伸;比如在踏上人行道边缘的时候,伸膝同时跖屈或者当踝关节完全跖屈时突然被施加巨大的背伸力,如运动员从高处跳下或坠落。
体格检查时可见局部肿胀瘀斑,可触及明显的压痛点和跟腱缺损;与对侧肢体相比,患侧踝被动背伸增加,跖屈减弱。双侧对比的Thompson试验常用于评估患者的主动跖屈功能,并能有效地去除长屈肌腱和趾长屈肌腱辅助跖屈引起的假阴性检查结果。评估患侧跟腱静息位张力也同样重要。检查时患者应保持俯卧位。静息位跟腱张力增加提示跟腱断裂可能增高。
2、影像学
由于该疾病主要根据典型病史及体格检查结果诊断,故仅在病史和体检结果不明确时,才需要进一步进行影像学检查。X线片中“Kager三角”、跟腱止点处高透亮区、跟骨撕脱骨折是典型的影像学表现。
超声检查能够确诊跟腱断裂,且比MRI检查更便宜。超声检查在跟腱断裂处显示出低回声区。Kotnis的动态超声研究表明:跟腱残端分离小于5mm的患者,通过非手术治疗或手术治疗后的跟腱再断裂发生率没有显著差别。虽然超声检查能够测量跟腱残端分离的距离,但是其可靠性与操作者的熟练度密切相关;在这方面其可信度不如MRI。虽然MRI更加昂贵和耗时,但在评估跟腱断裂程度和周围组织损伤情况方面更具优势。MRI在Tl、T2相上都会反映出跟腱断裂处的中断信号。
3、治疗
目前没有跟腱断裂治疗的金标准;但通常情况下,年轻患者和喜欢运动的患者更向于采用手术治疗(表16.4)。
| 表16.4 急性跟腱断裂的治疗结果 | ||||
| 强度 | 感染 | 再断裂 | 神经损伤 | |
| 切开 | 高 | 高 | 低 | 中等 |
| 经皮切口 | 高 | 低 | 低 | 高 |
| 微创切口 | 高 | 低 | 低 | 低 |
| 闭合 | 低 | 无 | 高 | 无 |
(1)非手术治疗
非手术治疗通常适用于老年患者、久坐患者或有并发症的患者。糖尿病、烟草依赖、静脉曲张、过度肥胖、肾衰竭、长期使用类固醇的患者,由于其手术干预的风险过高,而通常采用非手术治疗。非手术治疗主要是通过将踝关节制动于跖屈位,以便于减少断裂处缺损的长度。通过石膏或支具将踝关节固定于跖屈位的时间应不少于4周,随后应当继续固定于中立位4周。数据显示,使用功能性支具的患者发生跟腱再断裂的风险(2.4%)明显少于石膏制动的患者(12.4%)。
接受非手术治疗的患者跟腱再断裂发生率(12.7%)明显高于接受手术治疗的患者(3.5%);但非手术治疗也不会面临诸如腓肠神经损伤、切口愈合困难、瘢痕感觉过敏等手术并发症的困扰;在接受跟腱修复手术的患者中,有34%的患者会面临上述并发症的困扰。手术治疗有4%的切口感染风险,而非手术治疗则完全没有这样的问题。非手术治疗患者跖屈力更弱(非手术组为78%vs手术组为87%),重返运动场的可能性更低(非手术组为63%vs手术组为71%),接受非手术治疗的患者还会出现踝关节活动受限的问题。虽然手术治疗的并发症风险高,但是接受手术治疗的年轻、偏好运动的患者恢复伤前活动能力的可能性也高于接受非手术治疗的患者。
(2)手术治疗
手术治疗的方式包括:经皮修复、微创修复、大切口修复。手术治疗的目的是恢复跟腱的正常静息张力和长度、减少断端间的分离,并尽可能减少并发症的发生。与非手术治疗相比,手术治疗的优势在于更低的再断裂发生率、更早的功能恢复、更好的跟腱强度和更大的踝关节活动范围。外科手术修复能够获得更好的跟腱张力的原因在于:跟腱的胶原纤维组织在塑形阶段能够提供抗延展的张力,在成熟期则通过胶原蛋白交联增加跟腱的固有张力。手术治疗风险包括腓肠神经损伤、伤口愈合困难、浅部感染、瘢痕感觉过敏。
深静脉血栓形成(DVT)与跟腱断裂的相关性颇具争议。切口感染风险与肺栓塞风险成反比。考虑到这一并发症也会发生于一些相对健康的人,外科医师对此问题特别敏感。通过对跟腱断裂修复相关的DVT数据的研究,Pate等发现DVT的实际发生率比以前想象的要低,略低于0.5%。我们通常不会将使用药物预防DVT发生作为常规治疗,但在适当的时候会考虑这一手段。相对于标准切口手手术,小切口的微创手术比使用药物预防类似DVT更加有效。
经皮修复跟腱断裂的术式已经被证明手术时间更短、切口并发症更少(8.3%vs切开手术为26.1%)、术后感染率更低(vs切开手术为19.6%),而且伤口更加美观。Soubeyrand指出,超声能够协助定位所有缝合针的位置,并清楚地评估断端的间距。根据2005年Khan所做的一项荟萃分析研究,该术式术后跟腱再断裂率也优于切开修复(2.1%vs4.3%)。相对的,经皮修复的腓肠神经损伤率要高于切开修复(4.5%vs2.8%)。
跟腱断裂的切开修复需要以Krackow,Bunnell或Kessler缝合法实行端端吻合。Krackow缝合法能够有效地恢复跟腱的强度,但同时也有极高的并发症风险。术中可以通过腓肠肌翻转皮瓣、跖肌腱交叠修复或肌腱移植来增强跟腱的强度;但这些术式通常适用于跟腱再断裂或陈旧损伤的病例。另外,在缝合区域松解或切除跖肌腱能够减少术后粘连的发生率,同时增加跟腱的愈合率;如上所述,切开修复跟腱损伤腓肠神经的风险较低,但切口感染及再断裂的风险较高。
小切口修复术需要使用一种小型的经皮固定装置(图16.8)这样做能够保证在直视下准确地进行端端吻合,同时避免过度的软组织剥离,从而降低术后感染风险。现在已经发现,小切口修复术比常规的4线法Krackmv修复术失败率更高。
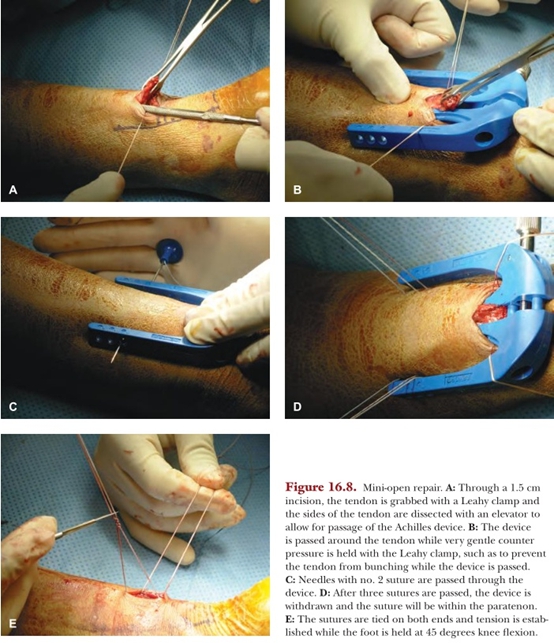
图16.8跟腱的微创修复。A.通过1.5cm长的切口,用菜希夹夹取跟腱残端,双侧穿线提拉固定,以便于使用跟腱缝合器.B.将跟腱缝合器轻柔置入跟腱两侧,注意用莱希夹保持跟腱的适当张力,避免 入跟腱缝合器时跟腱残端短缩缠绕;C.以2号缝线穿过跟腱;D.穿过3根缝线后,牵拉缝合器,将缝线固定于跟腱及跟腱周围组织;E.踝关节跖屈 45°,打结固定双侧缝线以恢复跟腱连续性。
术后康复包括一段较短吋间的制动和早期的功能锻炼。运动员通过术后强度逐渐增加的康复训练(表16.5)能够获得满意的功能,包括术后72小时开始的关节活动度训练、术后2周在CAM辅助下的离床训练以及术后6周的完全负重训练。通过这样的训练,93%的运动员都能在术后6个月左右重新参加比赛;其中仅2%~3%的患者会感觉跖屈力量减退。另外,术后先使用石膏制动再使用支具制动,比单纯使用传统石膏固定,能更好地降低术后粘连、感觉异常、瘢痕肥厚、感染等并发症的发生率。
| 表16.5 跟腱断裂的术后康复 | ||
| 时间 | 急性期处理 | 非急性期处理 |
| 0-2周 | 在石膏或护具固定下非负重 | 在石膏或护具固定下非负重 |
| 2-4周 | 在CAM辅助下的关节活动度训练 | 在石膏固定下非负重 |
| 4-6周 | 在CAM辅助下的部分负重 | 在CAM辅助下的关节活动度训练 |
| 6-8周 | 在CAM辅助下的足跟中立位 | 在CAM辅助下的部分负重 |
| 8-12周 | 穿着带跟鞋使足跟抬起 | 在CAM辅助下的足跟中立位 |
| 12-16周 | 一般的物理治疗 | 穿着带跟鞋使足跟抬起 |
| 4-6个月至恢复体育运动 | 依据具体运动进行物理治疗6-9个月 | 为期一般的物理治疗1年 |
二次校对完成于2018-3-3(说明:原著中文译本错误较多,使用中文译本请注意。)
Foot and Ankle SportS Medicine
Chapter 16 Achilles Pathology and Ruptures
Jonathan Kaplan
David B. thordarson
timothy p. Charlton